По оценке ВОЗ, сегодня в мире насчитывается не менее 130 млн. человек, болеющих сахарным диабетом, и это количество все увеличивается с каждым годом. Медики бьют настоящую тревогу, ведь по статистике означенной организации, число заболевших к 2025 году, может приблизится к 350 млн. человек. В России имеются данные о 2,5 млн. человек с сахарным диабетом. Причем, официальные сведения, на поверку оказываются заниженными в 2 или даже в 3 раза от реальной картины происходящего.
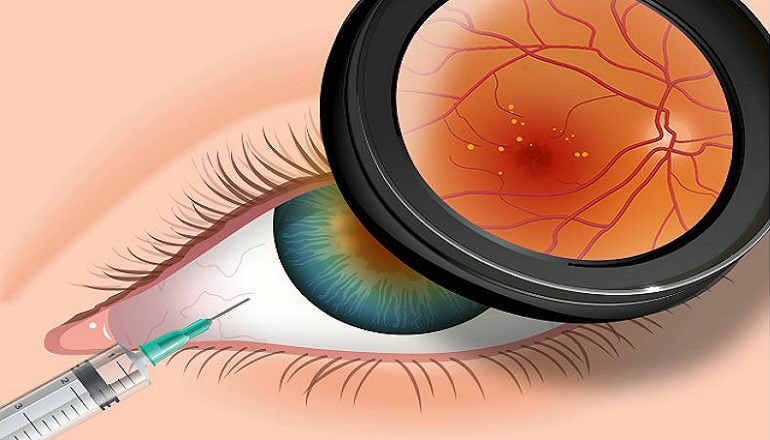
Одно из тяжелейших офтальмологических осложнений сахарного диабета – диабетическая ретинопатия (ДР), которая без лечения заканчивается необратимой слепотой. К настоящему моменту, специалисты активно разрабатывают и массово внедряют в клиническую практику эффективные консервативные методы лечения этого заболевания. Сочетание их со стандартной терапией способно значительно улучшить отдаленный прогноз.
К примеру, на данное время стали вполне доступны препараты-блокаторы эндотелиального фактора роста сосудов (VEGF). Ведь именно его принято считать, главной причиной начала неоваскуляризации, которая сопровождается гиперфильтрацией сосудов в сетчатку. Свет на проблему целесообразности применения этих препаратов у людей с сахарным диабетом может пролить тщательное изучение определенных свойств VEGF. Также детальное исследование должно быть проведено на предмет потенциально возможных осложнений, вызванных препаратами-блокаторами VEGF, которые способны нести реальную угрозу зрению и здоровью человека в целом.
Причины диабетической ретинопатии
Диабетическая ретинопатия возникает из-за хронической гипергликемии, запускающей целый ряд биохимических, патофизиологических, а также молекулярно-генетических механизмов. Их воздействие на сетчатку и приводит к ее патологическим изменениям. Гипергликемия становится основной причиной и прогрессирования ДР.
Высокий уровень сахара крови и вызываемый им окислительный стресс, а также отложение конечных продуктов гликирования и липидных нарушений, как и активация полиолового шунта, приводят к изменению эндотелиальных клеток сосудов сетчатки. Это происходит из-за возникновения определенных реакций, провоцирующих синтез цитокинов, факторов роста и липидов экстрацеллюлярного матрикса. Окончанием данного процесса становится дисфункция и гибель клеток с последующим распадом (апоптозом).
Вследствие таких изменений, сосуды начинают запустевать, отмирают перициты, плазма крови просачивается сквозь стенки сосудов, образуются кровоизлияния. Эти нарушения вызывают кислородное голодание сетчатки – гипоксии. Вызванные гипоксией повреждения ткани сетчатки активируют механизмы, повышающие внутри клеток уровень специфического белка HIF-1, отвечающего за генную транскрипцию. Рост уровня HIF-1 внутри клетки приводит к возрастанию транскрипции гена VEGF. Непосредственное выделение VEGF в межклеточный матрикс структуры, оказывает воздействие на эпителий, из-за чего возникает пролиферация, начинается рост новых сосудов и их регенерация.
VEGF: норма и патология
VEGF – выделенный впервые в 1983 году, фактор повышающий ломкость опухолевых сосудов. Это один из представителей семейства гомодимерных гликопротеинов, структура которого весьма близка структуре фактора роста тромбоцитов. Пять видов рецепторов тирозин-киназной активности имеют способность связываться с VEGF. Наиболее изученным на настоящий момент является VEGF-A, а также различные его изоформы.
При нарушениях в VEGFVEGFR системе возникают патологические и физиологические процессы, которые затрагивают: регуляцию женской репродукции, беременность, развитие эмбриона. Также они влияют на рост опухолей, заживляемость ран, развитие ишемических процессов и возникновение диабетической ретинопатии.
Особенно заметный биологический эффект VEGF выявлен при его взаимодействии с рецептором VEGF-R2 из группы трансмембранных тирозиновых киназ. Наиболее активно VEGF экспрессирует в изоформу VEGF165. Эта изоформа имеет наилучшие условия биодоступности и в том числе высокий биологический эффект. Интравитреальное введение данной формы показывает активное подавление патологической неовакуляризации, в свою очередь, практически не влияя на неоваскуляризацию физиологическую.
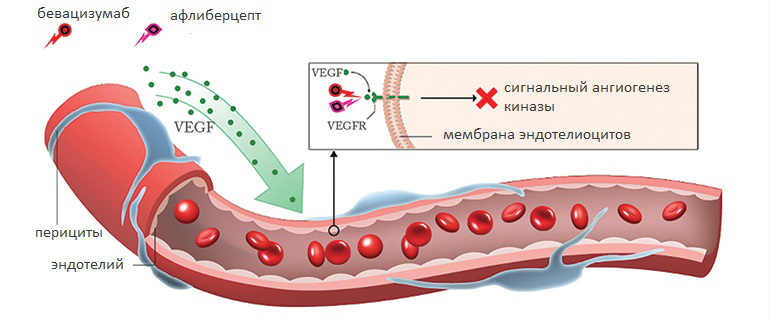
Действие VEGF особенно заметно, как в процессах эмбриогенеза, так и в раннем ангиогенезе новорожденных. Его работа у взрослых отмечается на различных уровнях: как эффективного вазодилятатора для сосудистой стенке, а также фактора, поддерживающего процесс выживания эндотелиальных клеток ткани. VEGF контролирует работу почечного гломерулярного фильтра и собственно сам гломерулогенез. Гломерулярный фильтр, при этом, напрямую воздействует на процессы регенерации клеток ткани мышц, помогает ремоделированию миокарда, стимулирует эндохондральное костеобразование. Действие его можно сравнить с действием хемоаттрактанта, активирующего мобилизацию клеток эндотелия костного мозга.
VEGF обладает не только физиологическим действием, хотя другие его полезные эффекты могут запускаться патогенетическими механизмами. Среди его полезных свойств: формирование коллатерального кровообращения. Именно такой, окольный ток крови при локальной ишемии, дает возможность выживать клеткам ткани и активизирует процессы регенерации при заживлении ран.
Синтез VEGF происходит на клеточном уровне в пигментном эпителии сетчатки и при сахарном диабете, это приводит к отеку сетчатки и неоваскуляризации с последующим ростом новых сосудов. У пациентов с диабетом первого типа выработка VEGF ведет к развитию пролиферативной диабетической ретинопатии, сопровождающейся с ростом новообразованных сосудов. А при диабете второго типа, данный процесс приводит к отеку сетчатки, что может стать причиной потери центрального зрения, когда патология задевает зону макулы.
Ингибиторы и блокаторы VEGF
В медицине сегодня существуют современные препараты с анти-VEGF свойствами, ни применяются для лечения метастазирующих опухолей у онкобольных. Это блокаторы и ингибиторы VEGF, которые по сути являются моноклональными антителами. Они избирательно связываются с VEGF и блокируют их. Такое действие подавляет рост новых сосудов в опухолях и лишает их способности развиваться.
Проведенные исследования сделали доступными данные о роли VEGF, как основного фактора диабетической ретинопатии. Это позволило предложить для ее лечения медикаментозные средства со свойствами блокирования VEGF – анти- VEGF препараты.
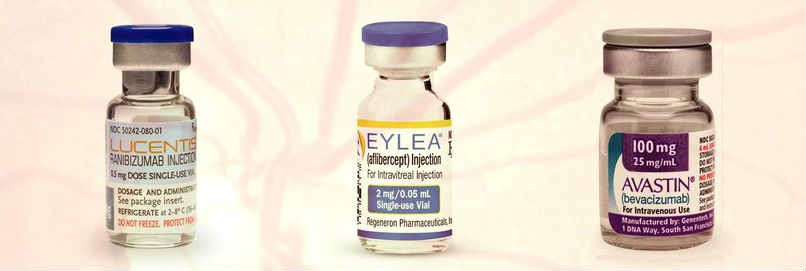
На данный момент офтальмологам доступны несколько таких препаратов: MACUGEN (Макуген, Макуджен), основное вещество которого пегаптаниб воздействует на VEGF165; Lucentis (Луцентис) с основным веществом ранибизумаб и Avastin (Авастин) с основным веществом бевацизумаб, способные подавляюще воздействовать на любые изоформы VEGF.
Действующее вещество Макугена пегаптаниб, является РНК-аптамером с максимально высоким сродством с VEGF165 связанным с полиэтиленгликолем. Применяемый в экспериментах с грызунами, как интравитреальные инъекции, он показал значительное подавление клеточной гиперфильтрации, неоваскуляризации и лейкостаза, возникавшие в сетчатке из-за действия VEGF. Благодаря такому действию, пегаптаниб и Макуген получили одобрение FDA (Food and Drug Administration, США) в 2004 году в терапии влажной формы возрастной макулярной дегенерации.
Луцентис с его действующим веществом ранибизумаб, создавался для предотвращения неоваскуляризации у пациентов с возрастной дегенерацией макулы. Достигается это посредством определенных изменений структуры длинноцепочечных крысиных моноклональных антител. Воздействие ранибизумаба подавляет свойства любых изоформ VEGF человека. В этом его кардинальное отличие от препарата Макуген на основе пегаптаниба. Проводившиеся эксперименты на нечеловекообразных обезьянах, когда у последних искусственно создавалась хориоидальная неоваскуляризация с помощью облучения лазером, доказали, что интравитреальные инъекции Луцентиса подавляли процесс образования сосудов и значительно снижали проницаемость тех, которые уже существуют. Поэтому и применения Луцентиса, как препарата для терапевтического лечения влажной формы ВМД в 2006 году получило одобрение FDA.
Авастин с действующим веществом бевацизумаб создавался с использованием лабораторных мышей, а точнее их антител к VEGF. Подобно ранибизумабу, он обладает способностью связывать все человеческие VEGF-изоформы. Препарат также эффективно останавливает процесс неоваскуляризации в терапии возрастной дегенерации макулы, хотя одобрения официальных органов он пока не получил. Причиной тому – недостаточное количество проведенных уже рандомизированных исследований его безопасности у людей.
Исследование анти-VEGF препаратов
При проведении исследований на самый оптимальный путь доставки препарата к месту поражения и эффективности его воздействия, были получены нижеследующие результаты.
Внутривенное введение. Внутривенное системное введение бевацизумаба для лечения офтальмологической патологии изучало только одно неконтролируемое исследование. Его участниками стали 18 пациентов, с диагностированной неоваскулярной влажной формой возрастной макулодистрофии. Доза препарата для введения составляла 5 мг⁄кг. Внутривенные вливания проводились 1, 2 и 3 раза с интервалом на отдых в 2 недели. По итогам, уже после 2 недель лечения, было выявлено повышение остроты зрения, с сохранением эффекта даже спустя 5-6 подконтрольных месяцев. Кроме того, к завершению исследования у всех участников отмечалось уменьшение толщины сетчатки и меньший ее отек. Дополнительную терапию получали только 6 из 18 наблюдавшихся участников. Правда, несмотря на получение положительной динамики проводимой терапии, в исследовании не изучались потенциально возможные ее осложнения и побочные эффекты.
Интравитреальное введение. В масштабных клинических исследованиях действия пегаптаниба и ранибизумаба у лиц с влажной формой возрастной дегенерации макулы были получены обнадеживающие результаты.
Правда, было установлено, что в сравнении с ранибизумабом (Луцентис), пегаптаниб (Макуген) показывает несколько меньшую эффективность. Но его применение значительно реже сопровождается осложнениями и побочными эффектами. Специалистам удалось выяснить, что применение ранибизумаба сопровождается определенным риском сердечнососудистых нарушений, включая и риск развития инсульта (подтверждено тремя исследованиями). Кроме того, иногда инъекции препарата вызывали кровотечения, хотя статистической значимости данное осложнение не имеет.
Полученные данные нескольких исследований позволили сделать вывод о результативности лечения анти-VEGF препаратами и у пациентов с сахарным диабетом. Одно из таких исследований объединило 172 человека участников с диабетическим отеком макулярной зоны. Лечение продолжалось 3, 5 месяца, к концу которых, пациенты получавшие пегаптаниб, имели лучшие результаты остроты зрения и меньшую толщину зоны макулы. Кроме того, дальнейшее лазерное лечение потребовалось значительно меньшему количеству участников из этой группы.
Еще одной областью применения анти-VEGF препаратов, а в частности в бевацизумаба (Авастин) в офтальмологии, является предоперационная терапия перед витрэктомией при диабетической ретинопатии пролиферативной формы.
Риски и осложнения анти-VEGF препаратов
Наилучший путь введения анти-VEGF препаратов – интравитреальная инъекция с проколом склеры внутрь стекловидного тела. Однако, при этом возможно проникновение действующего вещества в системный кровоток, что способно вызывать определенные осложнения и нежелательные последствия. К системным осложнениям этих препаратов можно отнести гипертензию и протеинурию, наиболее часто возникающих при лечении онкологических заболеваний. Собственно, повышение артериального давления, в этом случае, обусловлено недостаточностью синтеза оксида азота, который подавляется эндотелиальными клетками и повышением сопротивления периферического сосудистого кровотока. Хотя, возникновение гипертензии может указывать и на поражение функции почек.
Среди иных возможных осложнений анти-VEGF терапии, специалисты зачастую называют женское бесплодие, кровотечения из ЖКТ, плохую заживляемость ран, невозможность ремоделирования миокарда, регенерации мышц и формирования коллатерального кровообращения. Все эти негативные последствия
применения анти-VEGF препаратов, опасны в особенности для диабетиков.
Из наиболее часто возникающих офтальмологических осложнений терапии этими препаратами, стоит отметить: повреждение хрусталика, отслойку сетчатки, а также эндофтальмит. Хотя при интраокулярном введении анти-VEGF, серьезные негативные последствия возникают редко, но у пациентов с сахарным диабетом присутствует кумулятивный риск, так как данное заболевание, требуют проведения регулярных курсов терапевтического лечения в течение многих лет.
Негативные последствия самой инъекции, это далеко не единственные осложнения от введения препаратов с анти-VEGF действием. Присутствуют и другие нежелательные моменты подавления VEGF. Ведь данный фактор участвует в процессе формирования пигментного эпителия сетчатки, отвечает за жизнеспособность хориокапилляров и нейропротективный эффект, когда сетчатка находится в состоянии ишемии.
Интересно, что при применении анти-VEGF препарата пегаптаниб, не имеющего способности связываться с VEGF120, уменьшения числа ганглиозных клеток сетчатки не выявляется.
По данным других исследований, при интравитреальных инъекциях бевацизумаба, который способен блокировать все человеческие изоформы VEGF, на ганглиозные клетки сетчатки токсического воздействия также не происходит. Стоит упомянуть, что доказательств негативное влияния препаратов на сетчатку на сегодняшний день нет. Хотя, после введения бевацизумаба в тестах на крысах, при электронной микроскопии было выявлено разрушение митохондрий во внутреннем слое фоторецепторов с усиленным апоптозом.
До настоящего момента разработка препаратов-блокаторов VEGF, с эффектом подавления патологического воздействия VEGF, но сохраняющих нейропротективное действие, продолжаются. Именно им в будущем придется обеспечивать большую безопасность этих лекарств.
Интравитреальные инъекции препаратов с анти-VEGF действием являются надежным способом доставки действующего вещества напрямую к сетчатке. Об этом говорят данные клинических исследований и опыт лечения пациентов с возрастной дегенерацией макулы и пролиферативной формой диабетической ретинопатии. Однако стоит учитывать, что подобное введение – процедура инвазивная и связана с определенными рисками, такими как: кровотечение, эндофтальмит, отслойка сетчатки.
Сегодня в офтальмологической клинической практике широко применяются апробированные анти-VEGF препараты – MACUGEN (пегаптаниб), Lucentis (ранибизумаб) и Avastin (бевацизумаб). Правда их применение пока является лишь дополнением к традиционной терапии, позволяющее сделать отдаленный прогноз заболевания значительно лучше. Кроме того, при применении анти-VEGF препаратов в большинстве случаев нет необходимости в дальнейшем выполнять пациенту лазеркоагуляцию сетчатки.
В настоящее время анти-VEGF препараты нашли свое применение и в предоперационной подготовке больных перед антиглаукоматозными вмешательствами и витрэтомией, ведь они значительно снижают риск потенциально возможных послеоперационных осложнений.
И все же, применение анти-VEGF средств может стать причиной негативных последствий для здоровья человека, таких как активизации процесса сердечно-сосудистой патологии. В связи с этим, применение их в офтальмологии весьма актуально, но требует дополнительных исследований, целью которых будет не только выявление возможных положительных эффектов, но и определение потенциальных рисков системных осложнений. Ведь это особенно важно при лечении пациентов с сахарным диабетом.
Стоимость введения анти VEGF препаратов в Наро-Фоминске
Цены на процедуру интравитреального введения анти-VEGF препаратов в нашей клинике определяются, исходя из выбранного препарата, индивидуального состояния глаз пациента. С расценками Вы можете ознакомиться в разделе ЦЕНЫ.




